CNAS+����CMA����һ�����ֳ�����
2022/07/06


6��16�գ�����˼×��ҩ��Ժ×�������Ƴ���IHMD·2022��ǰϵ�н����Բ�����С���ҽ�I����е��ҵ���ߨ��������ܼ�������ʦ��Ϊ���������α����������ݽ�——��������û�ѧ����֧��ҽ����е����ѧ���ۡ�������������Ϣ�Ƽ�(�Ϻ�)����˾�ġ���Ƽ��ʦ��������Ϊ������ҽ����е��鼰֪ʶ��Ȩ����Ӧ�Բ��ԡ����ݽ��������2140�˴����߹�ע��


������û�ѧ����֧��ҽ����е����ѧ����

�� ��
��ҽ����е��ҵ�� �������ܼ�
�װ�����ͼ���ݿ�ҽ����е���ݿ����Ա����
�й�ʳƷҩƷ��ҵ������ȫ�ٽ���ҽ����е�ֻ�����ר�ҿ�ɡ�Ա
���˼�飺��ҽ����е��ѧ������ҩ����������о������⽵�������Լ����������Ԩw�ܼ��ȷ�����зḻ����Ŀʵ�����飬���뽨�����������ͼ���ݿ⡣�����ó�ҽ����е�ɵĻ�ѧ��������ҽ����е���ϻ�ѧ������ҩ�������ԡ������������о�����
���쵼�Ħ�ʵ�����Ŷ��Ѿ�����1000��ҽ�ơ���е������ҵ�������������Ϊ�߷���ҽ����е������Э���ǿ�ֲ�����Ѫ��ֲ������е�������ֲ������е���ۿ�ֲ����е��ѪҺ�����IJġ���ע���ߵ����߷���ҽ����е�ɹ����NMPA��FDA��CEע���걨��
PART 1
���չ��������е�����ѧ������
����ѧ���ۡ�����ı仯
��������ѧ�����������벻���Է�����ĸ��١��ͽ����
��ISO10993-1:2009 ��ISO 10993-1:2018 ���ָ��ԭ����̷�������ѧ��������������ѧ������ռ��Խ��Խ����ѧ�֡����������ڶԻ�ѧ���ʵļ�¼����������ֱ�ӽ��������۹���——����ѧ�������õ�����ѧ�����У��벻��������ѧ������2019�꣬������ѧ��ע��ֵTTC�����뵽ҽ����е�����������������Ӧ���У�ISO 10993-1(����-����)+ISO/TS 21726+ISO 10993-17��������+ISO 10993-18��������+ISO 10993-12���Ʊ��� �������γ�ϵͳ�Ե��������̡�����ѧ�����붾��������ӳ��ֵ���Ϻ�����Ρ�ѧ���۵�ʵ�����˸��õ�ץ�֡�
Ŀǰ��������ط��桢ָ��ԭ����Ȼ�ڡ������У�������ط�����������ϸ��¡�
�ӷ�������������Ҫ��
ͨ����������������ط����������Կ�����CE��FDA��CMDE��������ԡ�Ŀ������ê��������������ʹ���������и���ʵ��Ҫ��
��϶Է���������������������ķ�������Ļ����о������Կ���������ѧ�����Ѿ��ɴ�ͳ�����������Բ��ԣ�ת��Ϊ�Է硷�չ���Ϊ��������������ѧ����������ѧ�����������������������������ķ�ʽ�����������ѧ���ۡ�
����ѧ���۲�������
��ҽе�z��Ʒ��˵����ѧ��������������������ͬ�������������ִ�в��ԡ�
�Ƚ��л�ѧ�����u
ͨ����ѧ���ݵķ�������������Ʒ�п��ܺ��еĶ��������ʣ��õ��䶨�Զ������ݡ�
�ٽ��ж���ѧ����
���������ܺ��еĶ����������Ƿ������صĶ���ѧ����
��Զ���ѧ���ս�������������������
�γ�����ѧ�����۱���
PART 2
ISO 10993-18:2020 ��ѧ����
����
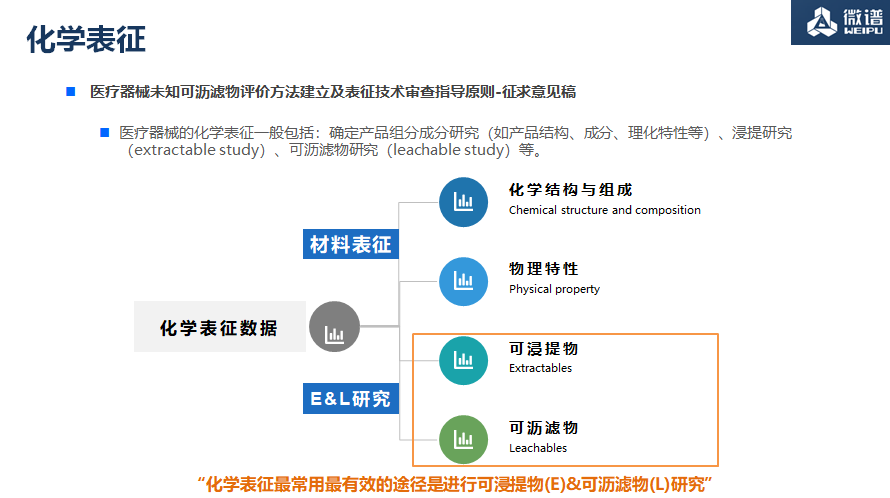
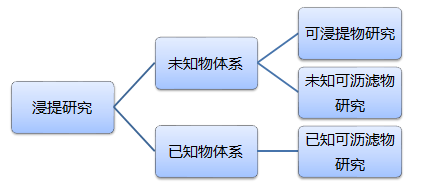
�ҹ��ġ�ҽ����еδ֪�����������۷��������������������ָ��ԭ��-��������塷��ȷָ����ҽ����е�Ļ�ѧ����һ�����——ȷ������Ʒ��ֳɷ��о������Ʒ�ṹ���ɷ֡��������Եȣ��������о���extractable study�������������о���leachable study����
tips����ѧ������ʵ��;���϶࣬��ʵ�ʲ����п��Ը��ݷ��յȼ��ж����鷽ʽ�������ṩ���о����ϡ�
��ѧ�����������ã�
1. ɸѡԭ�Ĩ���
2. ��������/��е��ͬ��
3. ���ⲿ������ѧ����
4. �����������ѧ�������
5. ֧���ٴ����v��
6. 3Rԭ���︣��
PART 3
�ɽ����E��&����������L���о�
��ض���
�ɽ����Extractable����ʹ��ʵ���ҽ��������ͽ�����ʶ�ҽ����е����е������Ͻ��н���ʱ�ͷŨ��������ʡ�
�������Leachable����ҽ����е���ٴ�ʹ�ù������ͷų��������ʡ�
��֪�������Target Leachables��
δ֪��������(Unspecified or Unknown Leachables)��
�ӻ��eѧ����������ά�ȷ���
E&L�о����̲���
��Ϣ�ռ�
�����������
��ֵȷ��
��������
���ݷ���/����ѧ����
����ѧ���������У���ҪӦ��MoSֵȥ���жϲ�Ʒ�Ķ���ѧ�����Ƿ��ܱ����ܡ�MoS��1����ζ�Ÿ����ʴ����Ķ���ѧ�����������⣬������ɱ����ܣ���Ҫ��һ�������������ݡ�������������ѧ�����Ľ��һ���̶���ȡ���ڿɽ����ﶨ�ԺͶ���/�붨���� ��ȷ�ԡ�
��λ��ȷ�����۽��
�Ʊ����ʵĽ���Һ
ѡ����ʵ�����
�ο�AET(�л���)+PDE��Ԫ�أ�+�߶ȹ�ע���ʽ����о�
�ɽ�����/δ֪���������ﶨ��
PART 4
��
���������о�����Ҫ��
���������ȷ��
������������������AL���Ľ���
����������ͷ����ⶨ��������ơޣ�����ʵ�������ƣ�
����ѧ��֤
��ѧ�����������ϱ����ͨuE&L�о�����ģ�飬���ӻ�ѧ����������ֻ�ܴﵽ���������������ã�������֧�Ų�Ʒ�ġ�ȫ�����ۣ�����ѧ��������Ϻ�࣬���ж��Զ������ݣ����л�����������������Ķ������ݣ��ܽϺõ�����γ��������ϡ�֧�ֽ������ϵĦ���ͬ�ԡ������������ѧ���顢����������������������ʱ���ٷ��������Ⲣ֧���ٴ����ۡ�